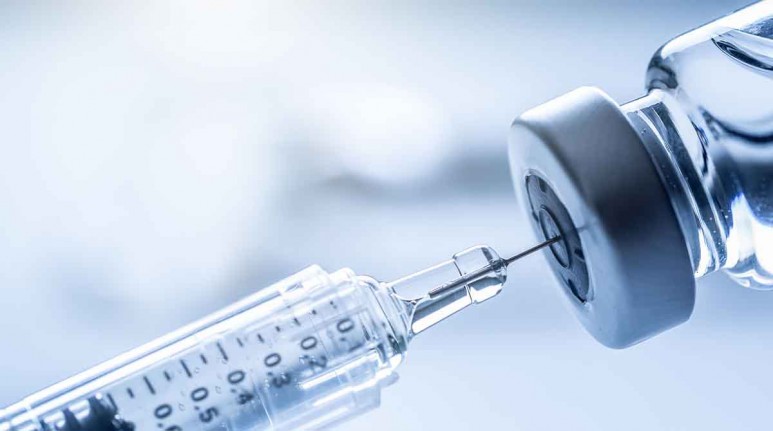
La vacuna bivalente 100% argentina contra COVID-19 fue presentada al mundo en la revista científica Nature
Por:
Daniela Blanco
Viernes 28 de
Julio 2023
El equipo de científicos argentinos a cargo del desarrollo publicó este viernes el paper con los detalles de la Fase I de la ARVAC Cecilia Grierson en la prestigiosa revista científica. Una innovación nacional desde el comienzo hasta el final, bajo la plataforma de proteínas recombinantes; que mostró protección contra distintas variantes del SARS-CoV-2 e inaugura una manera de producir y exportar ciencia local
El equipo científico del CONICET, la Universidad Nacional de San Martín (UNSAM) y la Fundación Cassará, que están desarrollando la vacuna ARVAC-Cecilia Grierson contra el COVID-19, presentaron hoy ante el mundo científico los detalles de la Fase I, al publicar un paper en la revista Nature. Allí abrieron la trastienda de la investigación de la nueva candidata vacunal, que ya se encuentra en etapa de ensayo clínico en humanos, tal como desde el inicio ha seguido de cerca Infobae y ha revelado todos los aspectos de este innovador proyecto de la ciencia argentina.
La noticia es muy relevante porque no solo servirá como adelanto científico, inscripto en las llamadas vacunas de segunda generación o dosis de refuerzo -destinadas a personas ya inmunizadas-; sino también porque inaugura una línea completa de innovación-desarrollo y producción en escala hecha en la Argentina: desde el comienzo de la molécula hasta la producción en escala. El producto ARVAC-Cecilia Grierson -bajo la plataforma de proteínas recombinantes- propulsa una ventana auspiciosa de exportación para la ciencia argentina; que seguramente servirá para terapéuticas para nuevas enfermedades.
Jorge Cassará, presidente de la Fundación Cassará y director del Laboratorio, dijo a Infobae tras la publicación, que “no son muchos los países que pueden diseñar, desarrollar y producir vacunas innovadoras. Este es un nuevo hito de un proyecto interdisciplinario de más de veinte instituciones públicas y privadas y constituye un ejemplo de lo que se puede lograr en Argentina cuando se trabaja en equipo”.
En el paper científico, los autores dieron cuenta de que el nuevo fármaco candidato a vacuna contra el COVID-19 basado en la variante Gamma del virus ha entrado en fase de ensayo clínico en humanos. La ARVAC CG contiene una proteína del virus (RBD) y un adyuvante de hidróxido de aluminio para estimular la respuesta inmune.
En la publicación, los expertos argentinos detallaron sus evaluaciones sobre seguridad y la capacidad de generar anticuerpos y células inmunes contra el virus en personas sanas que ya recibieron una vacuna primaria completa y compararon el efecto de este desarrollo con el de otra vacuna, la BNT162b2, es decir la de ARN mensajero de Pfizer/BioNTech. Además, destacaron que ARVAC-CG podrían ayudar a desarrollar una vacuna más efectiva contra las variantes del COVID-19.
Se trata así, de una vacuna bivalente contra el COVID-19 desarrollada íntegramente por científicos argentinos junto al Laboratorio Cassará, con apoyo de los ministerios de Salud y de Ciencia, Tecnología a Innovación (MinCyT), junto a la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i), sumados al esfuerzo conjunto de más de 20 instituciones públicas y privadas del país.
“La plataforma de desarrollo y producción montada servirá para producir vacunas proteicas seguras a gran escala, y en el caso de COVID-19 permite adecuarla a la nuevas variantes del virus para lograr una protección anual similar a la de gripe”, destacó Jorge Cassará, en diálogo con este medio.
Ya en 2021, Infobae había tenido un adelanto de boca de los líderes de este proyecto científico y también firmantes del paper publicado hoy: Juliana Cassataro, bióloga (UNSAM), doctora en Inmunología y líder del equipo UNSAM-CONICET y Juan Manuel Rodríguez, biólogo (UBA), y coordinador del área de I+D de biofármacos del Laboratorio y Fundación Pablo Cassará.
El pasado 18 de julio se había puesto un nuevo mojón en el próspero camino de ARVAC, ya que el equipo de investigación había completado el ensayo clínico de Fase III y anunciaba la presentación de la información correspondiente ante la ANMAT para continuar el proceso de evaluación y los pasos de rigor en busca de su aprobación.
La vacuna se inscribe en las llamadas de segunda generación o dosis de refuerzo destinadas a personas ya inmunizadas porque aparece en una etapa en la que la mayoría ya han recibido una o dos dosis. El inmunizante podría estar listo antes de fin de año. En una primera etapa estaría dirigido a menores de 60 años, mientras se siguen buscando voluntarios mayores de 60 para la continuidad del estudio, dijeron fuentes del MinCyT a este medio. Se prevé adaptar cada 4 meses la producción a las nuevas variantes y ofrecer un período de inmunidad contra el virus SARS-CoV-2 más largo que lo demostrado hasta ahora por las vacunas ARN mensajero.
Uno de quienes más se ha mostrado entusiasmado por este desarrollo ha sido el titular de esa cartera, Daniel Filmus, quien había expresado el “orgullo” que significa para la “ciencia argentina disponer de una vacuna nacional diseñada por nuestras científicas y científicos y producida por una empresa privada, lo que significa llevar la investigación y el desarrollo al servicio de las personas. Espero que antes de fin de año contemos con una vacuna íntegramente desarrollada en el país para atender a nuestra población”.
Cassataro dijo en su momento a Infobae que la vacuna “cumple el objetivo en cuanto a respuesta inmune contra las tres variantes probadas”. Ya en octubre de 2022, esta experta junto a Rodríguez, biólogo (UBA), y coordinador del área de I+D de biofármacos del Laboratorio y Fundación Pablo Cassará, habían delineado, en diálogo con Infobae, el extraordinario avance que significa esta vacuna para el desarrollo científico del país.
“Algo que aprendimos durante la pandemia fue a preguntarnos ¿qué capacidad productiva tenía la Argentina para hacer una vacuna a escala industrial? A nosotros no nos importaba tanto la innovación, sino un producto que sirva para el mayor número de personas”, reveló Cassataro.
Asimismo, ambos expertos destacaron que podrá actualizarse a medida que surjan nuevas variantes, porque conjuga una alta seguridad por su diseño, y además, al ser una proteína recombinante purificada y aislada, la generación del antígeno se hace fuera del cuerpo humano. La vacuna podrá tener una actualización de variantes ante un “escape inmunológico” o ante la aparición de una nueva variante en el país o la región.
“Este tipo de tecnología (producto basado en proteínas recombinantes) se guarda en la heladera y puede durar un año; por lo tanto, para la distribución en lugares remotos donde no tienen acceso a un freezer de -70° es sustancial. Y otro tema es que esta plataforma ya tiene la capacidad de manufactura en la región. Ya hay plantas que producen anticuerpos monoclonales y pueden hacerlas a lo largo y ancho del país”, explicó Rodríguez.
El paper publicado en Nature
En la introducción del trabajo publicado hoy, los expertos destacaron que la vacuna se ha probado como refuerzo en un estudio de Fase I en personas que ya habían recibido otras vacunas contra el COVID-19 y que los resultados preliminares mostraron que es segura y genera una fuerte respuesta de anticuerpos y células T contra el virus original y otras variantes, incluidas Delta y Ómicron. La vacuna es la primera que se diseña y produce íntegramente en Argentina y podría ser una opción para mejorar la protección contra el COVID-19 en los países de ingresos bajos y medianos, dijeron en el escrito.
La dosis de 50 µg fue más efectiva que la de 25 µg para inducir anticuerpos contra las variantes Ancestral y Omicron BA.1. Las tasas de seroconversión fueron altas para todas las variantes probadas y no hubo diferencias entre los individuos seronegativos o seropositivos, ni entre los voluntarios de diferente sexo o tiempo desde la vacunación primaria, afirmaron.
De esta forma, la fórmula, agregaron, logró seguridad y reactogenicidad en Fase I con dos grupos de dosis (25 y 50 µg). Los resultados mostraron que fue bien tolerada, con efectos adversos locales y sistémicos leves a moderados, más frecuentes tras la primera dosis. Los efectos adversos locales más comunes fueron malestar y dolor en el lugar de la inyección, mientras que los efectos adversos sistémicos más comunes fueron somnolencia, dolor de cabeza, mialgia y fatiga. Solo se reportó un caso de fiebre y no hubo efectos adversos graves ni de especial interés. Los valores de laboratorio anormales no fueron clínicamente significativos, expresaron.
Los resultados —agregaron— indicaron que la vacuna ARVAC CG induce niveles más altos de anticuerpos neutralizantes (inmunogenicidad) contra las variantes Gamma, Delta y Omicron que la formulación de Pfizer, mientras que los niveles contra la variante Ancestral son similares. Estos resultados se mantienen después de 28 días de la vacunación de refuerzo y en diferentes subgrupos de individuos.
Parte de las conclusiones de la investigación en palabras de los científicos: “Los principales hallazgos de este estudio son que la vacuna candidata ARVAC CG, cuando se administra como dosis de refuerzo, se tolera bien e induce una respuesta nAb sólida y amplia contra varios COV del SARS-CoV-2. Los resultados provisionales de este estudio de Fase I indican que la vacuna ARVAC CG administrada a personas que recibieron previamente un régimen de vacunación primaria completo tiene un perfil de seguridad y reactogenicidad clínicamente aceptable para ambas dosis de antígeno (25 μg y 50 μg)”.
La noticia es muy relevante porque no solo servirá como adelanto científico, inscripto en las llamadas vacunas de segunda generación o dosis de refuerzo -destinadas a personas ya inmunizadas-; sino también porque inaugura una línea completa de innovación-desarrollo y producción en escala hecha en la Argentina: desde el comienzo de la molécula hasta la producción en escala. El producto ARVAC-Cecilia Grierson -bajo la plataforma de proteínas recombinantes- propulsa una ventana auspiciosa de exportación para la ciencia argentina; que seguramente servirá para terapéuticas para nuevas enfermedades.
Jorge Cassará, presidente de la Fundación Cassará y director del Laboratorio, dijo a Infobae tras la publicación, que “no son muchos los países que pueden diseñar, desarrollar y producir vacunas innovadoras. Este es un nuevo hito de un proyecto interdisciplinario de más de veinte instituciones públicas y privadas y constituye un ejemplo de lo que se puede lograr en Argentina cuando se trabaja en equipo”.
En el paper científico, los autores dieron cuenta de que el nuevo fármaco candidato a vacuna contra el COVID-19 basado en la variante Gamma del virus ha entrado en fase de ensayo clínico en humanos. La ARVAC CG contiene una proteína del virus (RBD) y un adyuvante de hidróxido de aluminio para estimular la respuesta inmune.
En la publicación, los expertos argentinos detallaron sus evaluaciones sobre seguridad y la capacidad de generar anticuerpos y células inmunes contra el virus en personas sanas que ya recibieron una vacuna primaria completa y compararon el efecto de este desarrollo con el de otra vacuna, la BNT162b2, es decir la de ARN mensajero de Pfizer/BioNTech. Además, destacaron que ARVAC-CG podrían ayudar a desarrollar una vacuna más efectiva contra las variantes del COVID-19.
Se trata así, de una vacuna bivalente contra el COVID-19 desarrollada íntegramente por científicos argentinos junto al Laboratorio Cassará, con apoyo de los ministerios de Salud y de Ciencia, Tecnología a Innovación (MinCyT), junto a la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i), sumados al esfuerzo conjunto de más de 20 instituciones públicas y privadas del país.
“La plataforma de desarrollo y producción montada servirá para producir vacunas proteicas seguras a gran escala, y en el caso de COVID-19 permite adecuarla a la nuevas variantes del virus para lograr una protección anual similar a la de gripe”, destacó Jorge Cassará, en diálogo con este medio.
Ya en 2021, Infobae había tenido un adelanto de boca de los líderes de este proyecto científico y también firmantes del paper publicado hoy: Juliana Cassataro, bióloga (UNSAM), doctora en Inmunología y líder del equipo UNSAM-CONICET y Juan Manuel Rodríguez, biólogo (UBA), y coordinador del área de I+D de biofármacos del Laboratorio y Fundación Pablo Cassará.
El pasado 18 de julio se había puesto un nuevo mojón en el próspero camino de ARVAC, ya que el equipo de investigación había completado el ensayo clínico de Fase III y anunciaba la presentación de la información correspondiente ante la ANMAT para continuar el proceso de evaluación y los pasos de rigor en busca de su aprobación.
La vacuna se inscribe en las llamadas de segunda generación o dosis de refuerzo destinadas a personas ya inmunizadas porque aparece en una etapa en la que la mayoría ya han recibido una o dos dosis. El inmunizante podría estar listo antes de fin de año. En una primera etapa estaría dirigido a menores de 60 años, mientras se siguen buscando voluntarios mayores de 60 para la continuidad del estudio, dijeron fuentes del MinCyT a este medio. Se prevé adaptar cada 4 meses la producción a las nuevas variantes y ofrecer un período de inmunidad contra el virus SARS-CoV-2 más largo que lo demostrado hasta ahora por las vacunas ARN mensajero.
Uno de quienes más se ha mostrado entusiasmado por este desarrollo ha sido el titular de esa cartera, Daniel Filmus, quien había expresado el “orgullo” que significa para la “ciencia argentina disponer de una vacuna nacional diseñada por nuestras científicas y científicos y producida por una empresa privada, lo que significa llevar la investigación y el desarrollo al servicio de las personas. Espero que antes de fin de año contemos con una vacuna íntegramente desarrollada en el país para atender a nuestra población”.
Cassataro dijo en su momento a Infobae que la vacuna “cumple el objetivo en cuanto a respuesta inmune contra las tres variantes probadas”. Ya en octubre de 2022, esta experta junto a Rodríguez, biólogo (UBA), y coordinador del área de I+D de biofármacos del Laboratorio y Fundación Pablo Cassará, habían delineado, en diálogo con Infobae, el extraordinario avance que significa esta vacuna para el desarrollo científico del país.
“Algo que aprendimos durante la pandemia fue a preguntarnos ¿qué capacidad productiva tenía la Argentina para hacer una vacuna a escala industrial? A nosotros no nos importaba tanto la innovación, sino un producto que sirva para el mayor número de personas”, reveló Cassataro.
Asimismo, ambos expertos destacaron que podrá actualizarse a medida que surjan nuevas variantes, porque conjuga una alta seguridad por su diseño, y además, al ser una proteína recombinante purificada y aislada, la generación del antígeno se hace fuera del cuerpo humano. La vacuna podrá tener una actualización de variantes ante un “escape inmunológico” o ante la aparición de una nueva variante en el país o la región.
“Este tipo de tecnología (producto basado en proteínas recombinantes) se guarda en la heladera y puede durar un año; por lo tanto, para la distribución en lugares remotos donde no tienen acceso a un freezer de -70° es sustancial. Y otro tema es que esta plataforma ya tiene la capacidad de manufactura en la región. Ya hay plantas que producen anticuerpos monoclonales y pueden hacerlas a lo largo y ancho del país”, explicó Rodríguez.
El paper publicado en Nature
En la introducción del trabajo publicado hoy, los expertos destacaron que la vacuna se ha probado como refuerzo en un estudio de Fase I en personas que ya habían recibido otras vacunas contra el COVID-19 y que los resultados preliminares mostraron que es segura y genera una fuerte respuesta de anticuerpos y células T contra el virus original y otras variantes, incluidas Delta y Ómicron. La vacuna es la primera que se diseña y produce íntegramente en Argentina y podría ser una opción para mejorar la protección contra el COVID-19 en los países de ingresos bajos y medianos, dijeron en el escrito.
La dosis de 50 µg fue más efectiva que la de 25 µg para inducir anticuerpos contra las variantes Ancestral y Omicron BA.1. Las tasas de seroconversión fueron altas para todas las variantes probadas y no hubo diferencias entre los individuos seronegativos o seropositivos, ni entre los voluntarios de diferente sexo o tiempo desde la vacunación primaria, afirmaron.
De esta forma, la fórmula, agregaron, logró seguridad y reactogenicidad en Fase I con dos grupos de dosis (25 y 50 µg). Los resultados mostraron que fue bien tolerada, con efectos adversos locales y sistémicos leves a moderados, más frecuentes tras la primera dosis. Los efectos adversos locales más comunes fueron malestar y dolor en el lugar de la inyección, mientras que los efectos adversos sistémicos más comunes fueron somnolencia, dolor de cabeza, mialgia y fatiga. Solo se reportó un caso de fiebre y no hubo efectos adversos graves ni de especial interés. Los valores de laboratorio anormales no fueron clínicamente significativos, expresaron.
Los resultados —agregaron— indicaron que la vacuna ARVAC CG induce niveles más altos de anticuerpos neutralizantes (inmunogenicidad) contra las variantes Gamma, Delta y Omicron que la formulación de Pfizer, mientras que los niveles contra la variante Ancestral son similares. Estos resultados se mantienen después de 28 días de la vacunación de refuerzo y en diferentes subgrupos de individuos.
Parte de las conclusiones de la investigación en palabras de los científicos: “Los principales hallazgos de este estudio son que la vacuna candidata ARVAC CG, cuando se administra como dosis de refuerzo, se tolera bien e induce una respuesta nAb sólida y amplia contra varios COV del SARS-CoV-2. Los resultados provisionales de este estudio de Fase I indican que la vacuna ARVAC CG administrada a personas que recibieron previamente un régimen de vacunación primaria completo tiene un perfil de seguridad y reactogenicidad clínicamente aceptable para ambas dosis de antígeno (25 μg y 50 μg)”.