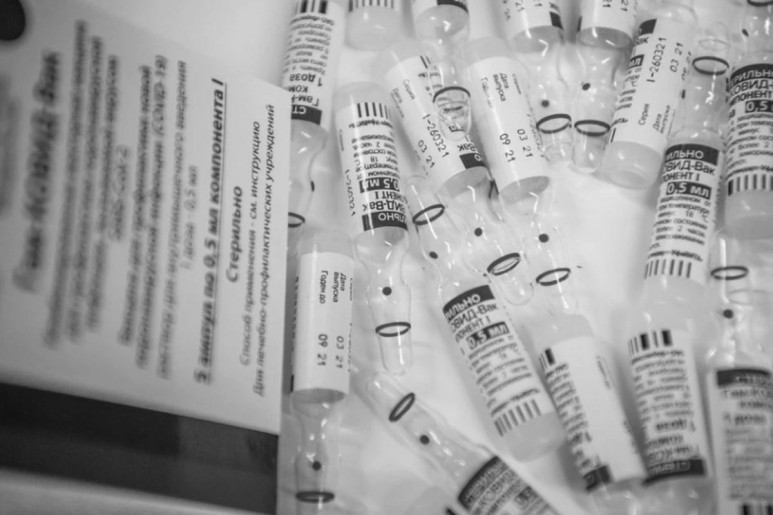
Por cuestiones técnicas detectadas durante una inspección en Rusia la OMS suspende la aprobación de Sputnik V
Por:
Pablo Sigal
Martes 14 de
Septiembre 2021
La vacuna Sputnik V es una de las vacunas más efectivas y al mismo tiempo es la más controvertida. Su proceso de autorización en la Organización Mundial de la Salud (OMS) empezó a comienzos de este año y aún hoy no hay novedades.
Desde el Fondo Ruso de Inversión Directa no surge información nueva sobre el avance de ese trámite, que según el organismo sanitario internacional está virtualmente suspendido.
La vacuna es utilizada en 70 países, entre ellos la Argentina, y no cuenta con la homologación de la OMS, como sí la tienen otras vacunas como Pfizer, Moderna, AstraZeneca, Janssen, Sinopharm y Sinovac. En nuestro país ya se utilizaron más de 15 millones de vacunas rusas, de los cuales casi 11 millones corresponden al componente 1 y el resto al componente 2.
La advertencia sobre la suspensión del proceso de homologación la dio Jarbas Barbosa, subdirector de la Organización Panamericana de la Salud (OPS), oficina regional de la OMS. Fue una declaración en la última conferencia de prensa que dio el organismo: “El proceso de autorización de uso de emergencia de la vacuna Sputnik V por parte de la OMS está suspendido desde el mes de junio”, dijo el funcionario.
La OMS pidió más información al Instituto Gamaleya para continuar con el proceso administrativo y sanitario. El grupo independiente de expertos en vacunas de la OMS se encarga de analizar la información de los ensayos clínicos y de verificar además las condiciones de producción de la vacuna.
El inconveniente surgió cuando la OMS inspeccionó las instalaciones del Instituto Gamaleya y halló algunos déficits. Dmitry Peskov, vocero del Kremlin, había asegurado en ese momento que hubo “algunas deficiencias identificadas por el grupo de inspección. Se tuvieron en cuenta y se cambió todo lo que había que cambiar”.
Pero según la OPS las cosas no son tan sencillas. Barbosa detalló que “esta suspensión se dio porque se encontró en una planta productora de las vacunas Sputnik condiciones que no son las adecuadas para las buenas prácticas de producción. Entonces, está suspendido (el proceso) aguardando que el productor adopte las medidas necesarias para que otra inspección pueda ir y certificar que las condiciones son las adecuadas”.
La homologación de la OMS no es requisito indispensable para que una vacuna sea utilizada en un país. Pero hay naciones que toman como referencia las recomendaciones de la OMS, la Administración de Drogas y Alimentos (FDA) y la Agencia Europea de Medicamentos (EMA) para otorgar permisos de emergencia.
Que la vacuna esté aprobada en otros países es clave para que aquellos que están inmunizados con la Sputnik V obtengan el aval inmunitario para circular libremente. De otro modo pueden surgir trabas e inconvenientes. En Europa, por ahora sólo Hungría y Eslovaquia la aprobaron por su cuenta, más allá del visto bueno de la Agencia Europea del Medicamento (EMA).
Barbosa agregó que “hasta ahora la vacuna Sputnik no puede ser adquirida por el fondo rotativo de la OPS o por el mecanismo Covax. Hay países que tomaron la decisión de certificar la vacuna, es una decisión de cada país. Hasta el momento no tenemos una fecha de cuándo este proceso se va a concretar”.
Un artículo publicado por The Moscow Times, el último viernes, subrayó que la OMS y la EMA siguen aguardando la información solicitada para poder avanzar con una eventual autorización.
El “conflicto” data de enero, cuando el organismo sanitario mundial dijo que había identificado ciertos problemas en la implementación de medidas adecuadas para “mitigar los riesgos de contaminación cruzada”, como también la “validación apropiada de filtración estéril" de la vacuna Sputnik V.
La inspección se llevó a cabo para evaluar si la fábrica estaba operando de acuerdo con las llamadas Buenas Prácticas de Manufactura (GMP), un conjunto de pautas regulatorias que dictan los estándares que deben cumplir los sitios involucrados en la fabricación de productos farmacéuticos.
La planta Pharmstandard, donde la OMS hizo su inspección, explicó que los cuestionamientos fueron "problemas técnicos, principalmente relacionados con una de las líneas de llenado".
Los voceros agregaron que la planta es responsable de llenar el líquido de la vacuna en viales, y que el antígeno se produce en una instalación diferente. La compañía aclaró que la OMS "no planteó ninguna pregunta sobre la seguridad y eficacia de la vacuna producida y terminada", ni "identificó ningún problema crítico con la producción real de la vacuna, la calidad, los estudios clínicos o los posibles efectos secundarios".
En Sudamérica, Sputnik V había tenido problemas en Brasil. A fines de abril, la agencia sanitaria Anvisa había emitido una opinión negativa, a partir de la solicitud de diez estados para importar la vacuna rusa. Señaló fallas técnicas en los estudios y en la producción del vacuna.
Esas cuestiones, según se afirmó, podían llegar a presentar riesgos para la seguridad y la calidad del agente inmunizante. Finalmente en junio el Ministerio de Salud brasileño allanó el camino para que el inoculante pudiera ingresar al país, tras un nuevo informe técnico de Anvisa y el Ministerio de Salud de Rusia .
La vacuna es utilizada en 70 países, entre ellos la Argentina, y no cuenta con la homologación de la OMS, como sí la tienen otras vacunas como Pfizer, Moderna, AstraZeneca, Janssen, Sinopharm y Sinovac. En nuestro país ya se utilizaron más de 15 millones de vacunas rusas, de los cuales casi 11 millones corresponden al componente 1 y el resto al componente 2.
La advertencia sobre la suspensión del proceso de homologación la dio Jarbas Barbosa, subdirector de la Organización Panamericana de la Salud (OPS), oficina regional de la OMS. Fue una declaración en la última conferencia de prensa que dio el organismo: “El proceso de autorización de uso de emergencia de la vacuna Sputnik V por parte de la OMS está suspendido desde el mes de junio”, dijo el funcionario.
La OMS pidió más información al Instituto Gamaleya para continuar con el proceso administrativo y sanitario. El grupo independiente de expertos en vacunas de la OMS se encarga de analizar la información de los ensayos clínicos y de verificar además las condiciones de producción de la vacuna.
El inconveniente surgió cuando la OMS inspeccionó las instalaciones del Instituto Gamaleya y halló algunos déficits. Dmitry Peskov, vocero del Kremlin, había asegurado en ese momento que hubo “algunas deficiencias identificadas por el grupo de inspección. Se tuvieron en cuenta y se cambió todo lo que había que cambiar”.
Pero según la OPS las cosas no son tan sencillas. Barbosa detalló que “esta suspensión se dio porque se encontró en una planta productora de las vacunas Sputnik condiciones que no son las adecuadas para las buenas prácticas de producción. Entonces, está suspendido (el proceso) aguardando que el productor adopte las medidas necesarias para que otra inspección pueda ir y certificar que las condiciones son las adecuadas”.
La homologación de la OMS no es requisito indispensable para que una vacuna sea utilizada en un país. Pero hay naciones que toman como referencia las recomendaciones de la OMS, la Administración de Drogas y Alimentos (FDA) y la Agencia Europea de Medicamentos (EMA) para otorgar permisos de emergencia.
Que la vacuna esté aprobada en otros países es clave para que aquellos que están inmunizados con la Sputnik V obtengan el aval inmunitario para circular libremente. De otro modo pueden surgir trabas e inconvenientes. En Europa, por ahora sólo Hungría y Eslovaquia la aprobaron por su cuenta, más allá del visto bueno de la Agencia Europea del Medicamento (EMA).
Barbosa agregó que “hasta ahora la vacuna Sputnik no puede ser adquirida por el fondo rotativo de la OPS o por el mecanismo Covax. Hay países que tomaron la decisión de certificar la vacuna, es una decisión de cada país. Hasta el momento no tenemos una fecha de cuándo este proceso se va a concretar”.
Un artículo publicado por The Moscow Times, el último viernes, subrayó que la OMS y la EMA siguen aguardando la información solicitada para poder avanzar con una eventual autorización.
El “conflicto” data de enero, cuando el organismo sanitario mundial dijo que había identificado ciertos problemas en la implementación de medidas adecuadas para “mitigar los riesgos de contaminación cruzada”, como también la “validación apropiada de filtración estéril" de la vacuna Sputnik V.
La inspección se llevó a cabo para evaluar si la fábrica estaba operando de acuerdo con las llamadas Buenas Prácticas de Manufactura (GMP), un conjunto de pautas regulatorias que dictan los estándares que deben cumplir los sitios involucrados en la fabricación de productos farmacéuticos.
La planta Pharmstandard, donde la OMS hizo su inspección, explicó que los cuestionamientos fueron "problemas técnicos, principalmente relacionados con una de las líneas de llenado".
Los voceros agregaron que la planta es responsable de llenar el líquido de la vacuna en viales, y que el antígeno se produce en una instalación diferente. La compañía aclaró que la OMS "no planteó ninguna pregunta sobre la seguridad y eficacia de la vacuna producida y terminada", ni "identificó ningún problema crítico con la producción real de la vacuna, la calidad, los estudios clínicos o los posibles efectos secundarios".
En Sudamérica, Sputnik V había tenido problemas en Brasil. A fines de abril, la agencia sanitaria Anvisa había emitido una opinión negativa, a partir de la solicitud de diez estados para importar la vacuna rusa. Señaló fallas técnicas en los estudios y en la producción del vacuna.
Esas cuestiones, según se afirmó, podían llegar a presentar riesgos para la seguridad y la calidad del agente inmunizante. Finalmente en junio el Ministerio de Salud brasileño allanó el camino para que el inoculante pudiera ingresar al país, tras un nuevo informe técnico de Anvisa y el Ministerio de Salud de Rusia .